日期:2025-08-07 02:56:58
*仅供医学专业人士阅读参考科云汇
德曲妥珠单抗改写难治性HER2变异晚期NSCLC治疗结局,实现脑转移显著消退与长生存获益。
肺癌长期居我国恶性肿瘤发病与死亡首位,其中(NSCLC)占比高达85%[1],HER2作为重要驱动基因,其临床价值日益凸显。然而,传统抗HER2靶向治疗在HER2突变晚期NSCLC患者中的疗效有限,客观缓解率(ORR)不足30%[2]。因此,探索针对HER2突变晚期肺癌的更有效、精准治疗策略尤为迫切。以德曲妥珠单抗为代表的新一代抗体偶联药物(ADC),凭借其独特结构设计、作用机制及DESTINY-Lung系列研究提供的循证证据,正逐步确立其在HER2突变晚期NSCLC治疗中的地位,有望为该领域治疗模式带来全面革新。
在此背景下,本文聚焦两例典型HER2变异晚期NSCLC患者的全程管理实践,由解放军总医院王李杰教授系统解析其精准诊疗路径,为临床提供关键参考。
病例分享一:德曲妥珠单抗治疗左肺腺癌伴全身多发转移且多线治疗进展的高龄患者
■诊疗过程
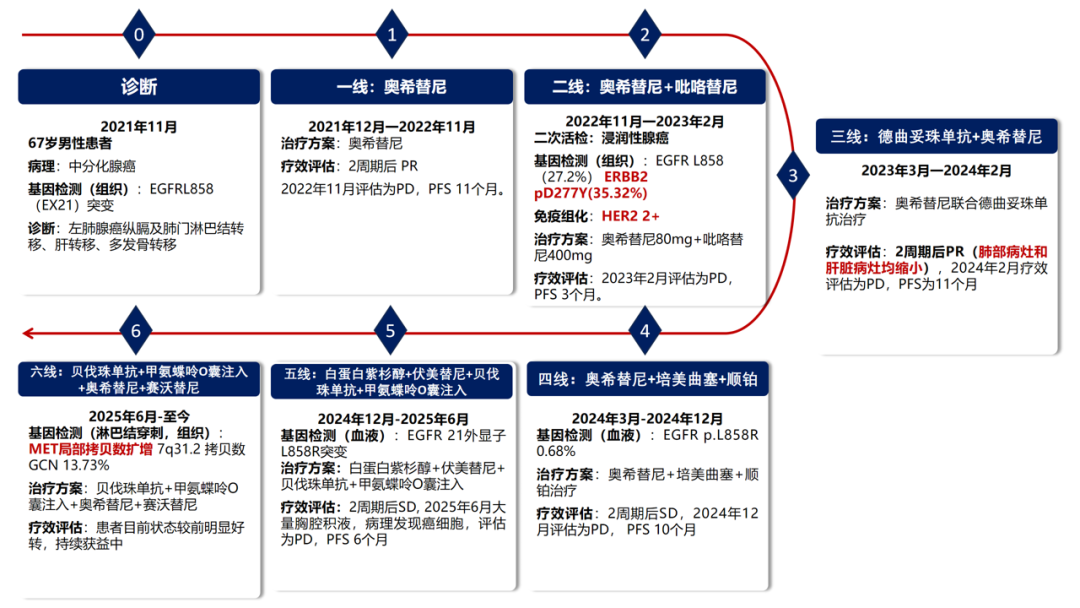
■基本情况
患者男,67岁,2021年10月因腰部疼痛起病,主诉为“确诊左肺腺癌多发转移近3年”。
■辅助检查
PET-CT检查(2021年11月19日):考虑左肺上叶恶性肿瘤,纵膈及左肺门淋巴结转移,肝内多发转移,全身多发骨转移。
CT引导下穿刺活检(2021年11月24日):(肺组织)中分化腺癌。
基因检测:EGFR L858(EX21)突变。
临床诊断:左肺腺癌伴纵膈及肺门淋巴结转移、肝转移、多发骨转移。
■一线治疗
治疗方案:2021年12月-2022年11月,给予奥希替尼治疗。
疗效评估:2022年2月疗效评估为部分缓解(PR),2022年11月疗效评估为疾病进展(PD)。
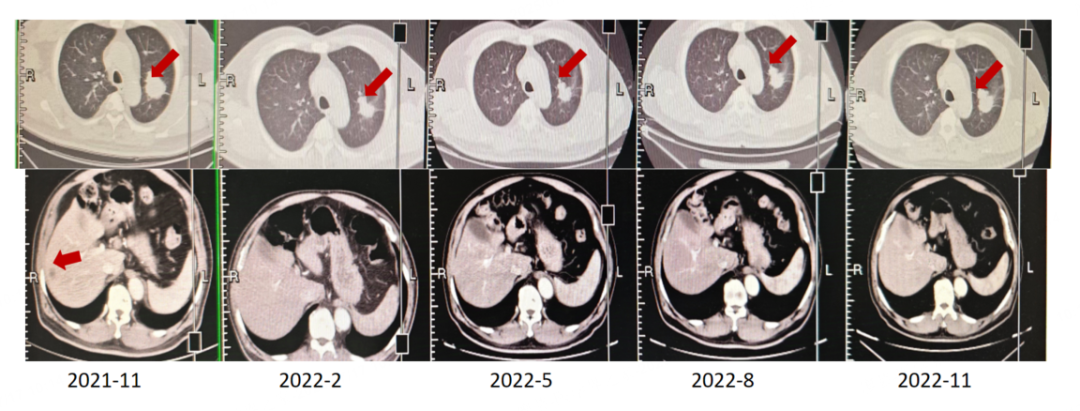
图1. 一线治疗的疗效评估结果
■二线治疗
二次活检(2022年11月4日):浸润性腺癌。
基因检测(组织):EGFR L858(27.2%),ERBB2 pD277Y(35.32%)。
病理组织加做免疫组化(2023年2月):HER2(2+)。
治疗方案:2022年11月-2023年2月,给予奥希替尼 80mg+吡咯替尼 400mg治疗。
疗效评估:2023年2月疗效评估为PD,无进展生存期(PFS)仅3个月
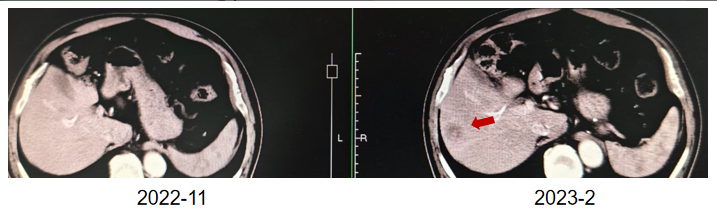
图2.二线治疗的疗效评估结果
■三线治疗
治疗方案:2023年3月-2024年2月,奥希替尼 80mg+德曲妥珠单抗 300mg。
疗效评估:
2023年4月肺部及肝脏病灶较前均缩小,疗效评估为PR。
2023年9月肺部病灶较前相仿,疗效评估为PR。
2023年11月肺部病灶较前缩小,肝脏病灶较前减小,疗效评估为PR。
2024年2月肝脏病灶较前增大,多个肿瘤标记物较前持续升高,疗效评估为PD。

图3.三线治疗的疗效评估结果
■四线治疗
基因检测(2024年2月):EGFR p.L858R 0.68%科云汇。
治疗方案:2024年3月,给予奥希替尼+培美曲塞+顺铂治疗
疗效评估:2024年5月 疗效评估为疾病稳定(SD),2024年12月肺部病灶较前增大,出现脑部症状,考虑脑膜转移,疗效评估为PD。
基因检测(2024年11月):EGFR 21外显子L858R突变
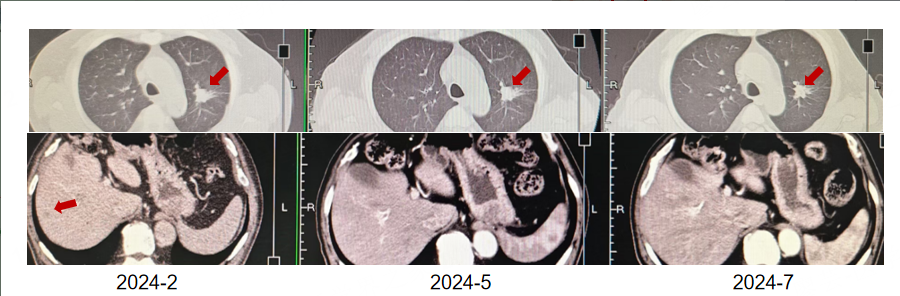
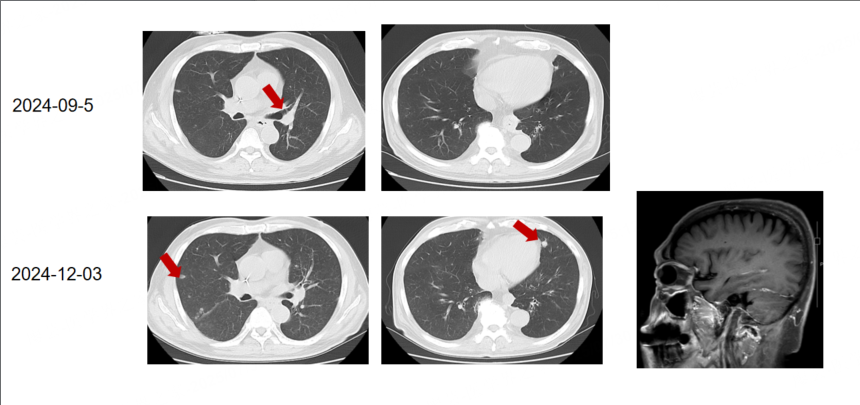
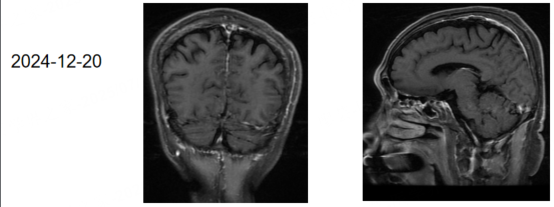
图4. 四线治疗的疗效评估结果
■五线治疗
治疗方案:2024年12月,行紫杉醇(白蛋白结合型)+伏美替尼+贝伐珠单抗方案治疗4周期。2025年1月行Ommaya囊植入,并行甲氨蝶呤Ommaya囊注入。
疗效评估:2周期后SD;2025年6月外院CT反复大量胸腔积液合并肺炎,病理检查发现癌细胞,疗效评估为PD。
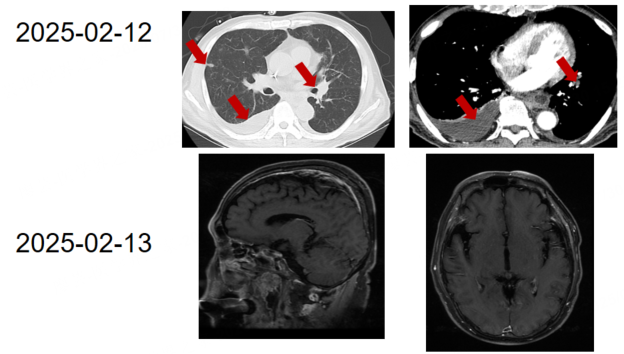
图5. 五线治疗的疗效评估结果
■六线治疗
基因检测(淋巴结穿刺,组织;2025年6月16日):EGFR c.2573.T>G p.L858R exon21 突变丰度53.86%;ERBB2 c.829 G>T p.D277Y exon7 突变丰度 68.45%;MET局部拷贝数扩增7q31.2 拷贝数GCN 13.73%。
治疗方案:2025年6月,行贝伐珠单抗+甲氨蝶呤O囊注入+奥希替尼+赛沃替尼治疗。
疗效评估:目前患者自诉状态较前明显好转,持续获益中。
■病例总结
67岁男性患者,诊断为左肺腺癌伴纵隔及肺门淋巴结转移、肝转移、多发骨转移,并伴有EGFR L858(EX21)突变。
一线治疗采用奥希替尼,一线PFS为11个月。
二线治疗采用奥希替尼+吡咯替尼,二线PFS仅为3个月。
三线治疗前10周期采用奥希替尼+德曲妥珠单抗治疗,治疗1个月后疗效评估即达PR,并维持PR达11个月,11个月后疗效评估为PD。治疗期间整体耐受性良好,三线PFS长达11个月。
四线治疗采用奥希替尼+培美曲塞+顺铂治疗,第4、6周期疗效评估为SD,第8周期评估为PD。
五线治疗采用行紫杉醇(白蛋白结合型)+伏美替尼+贝伐珠单抗+甲氨蝶呤O囊注入方案治疗4周期。治疗2周期后SD,随后PD。
六线治疗行贝伐珠单抗+甲氨蝶呤O囊注入+奥希替尼+赛沃替尼治疗。目前患者自述状态较前好转,持续获益中。
病例分享二:德曲妥珠单抗治疗多发转移肺腺癌伴HER2基因扩增和融合
■诊疗过程
■基本情况
患者男,确诊左肺腺癌伴双肺转移4年余。
■辅助检查
胸部CT检查(2021年5月):1、考虑左肺上叶周围型肺癌(左肺上叶前段见约28mmx33mm肿块)伴双肺、胸膜、双肺门及纵隔多发转移;双肺癌性淋巴管炎。2、双肺散在陈旧性病灶;右侧胸膜钙化。
肿瘤标志物(2021年5月):CYFRA21-1、NSE升高。
病理:肺原发性低分化腺癌。
免疫组化:TTF-1(+++)、NapsinA(+)、CgA(-)、syn(-)、Ki-67(35%+)、P63(-)、P40(-)、CK7(+++)、CK20(-)、villin(-)、CD56(-)。
基因检测:EGFR p.L858R第21外显子错义突变,HER2基因扩增,STARD3-ERBB2融合。
临床诊断:左肺低分化腺癌(IV期),纵隔及左侧锁骨上窝淋巴结转移、双肺多发转移、双侧胸膜转移、脑转移、癌性淋巴管炎。
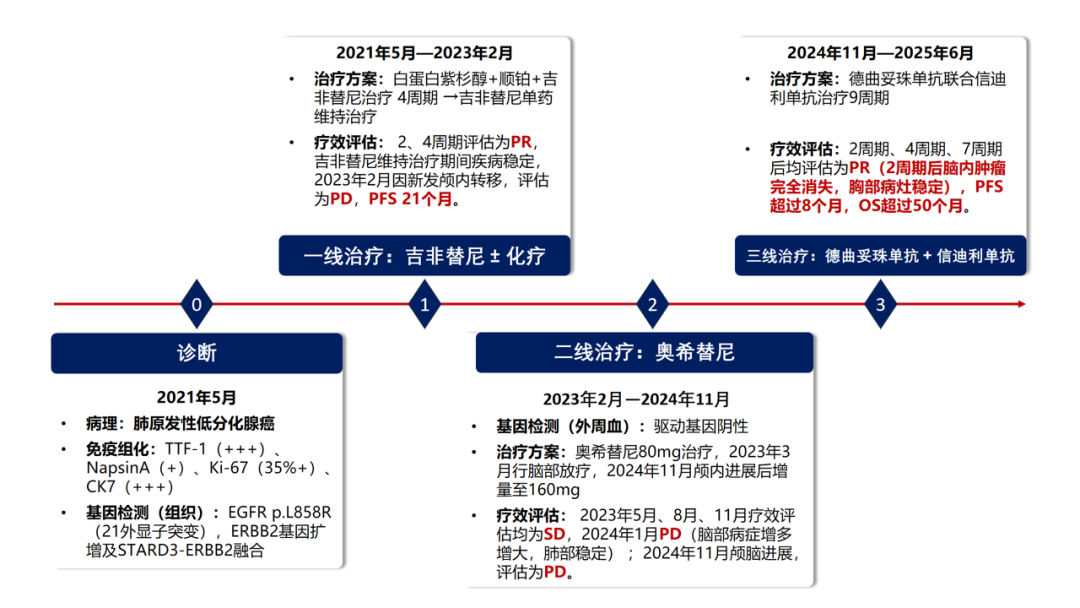
■一线治疗
治疗方案:2021年5月至7月,行4周期白蛋白紫杉醇+顺铂+吉非替尼联合治疗科云汇,后予吉非替尼单药维持治疗至2023年2月。
疗效评估:治疗2、4个周期后疗效评估为PR;吉非替尼维持治疗期间定期复查示疾病稳定。2023年2月23日颅脑磁共振(MRI)提示新发转移灶,评估为PD;外周血基因检测未检出驱动基因突变(MSS),PFS为21个月。
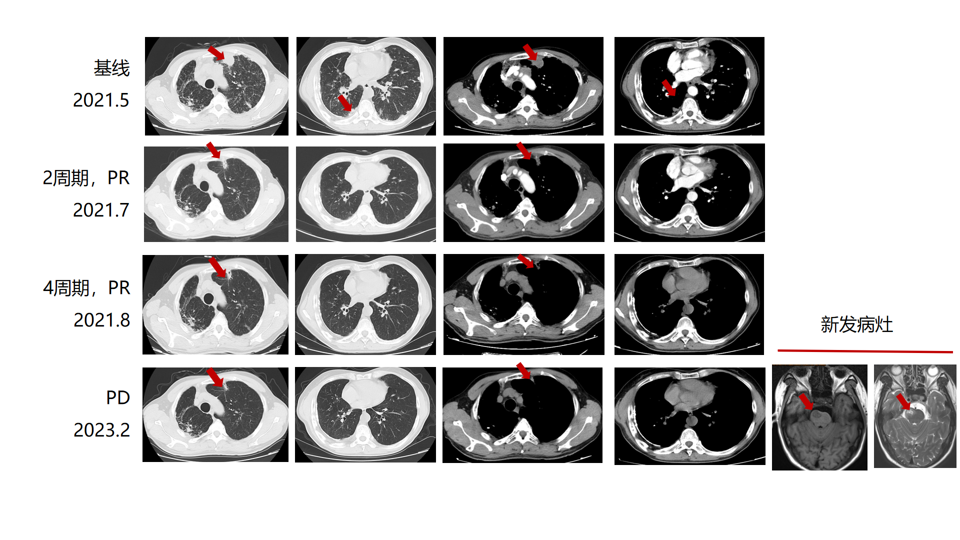
图6. 一线治疗前后影像学评估结果
■二线治疗
基因检测(外周血):驱动基因阴性。
治疗方案:2023年2月27日起口服奥希替尼80mg,2024年1月因颅内进展增量至160mg,治疗至2024年11月。
治疗经过:2023年3月行脑部放疗。
疗效评估:2023年5月、8月、11月疗效评估均为SD,2024年1月PD(脑部病症增多增大,肺部稳定);2024年11月颅脑MRI示病灶增多增大,评估为PD,且因病灶多发不宜放疗。
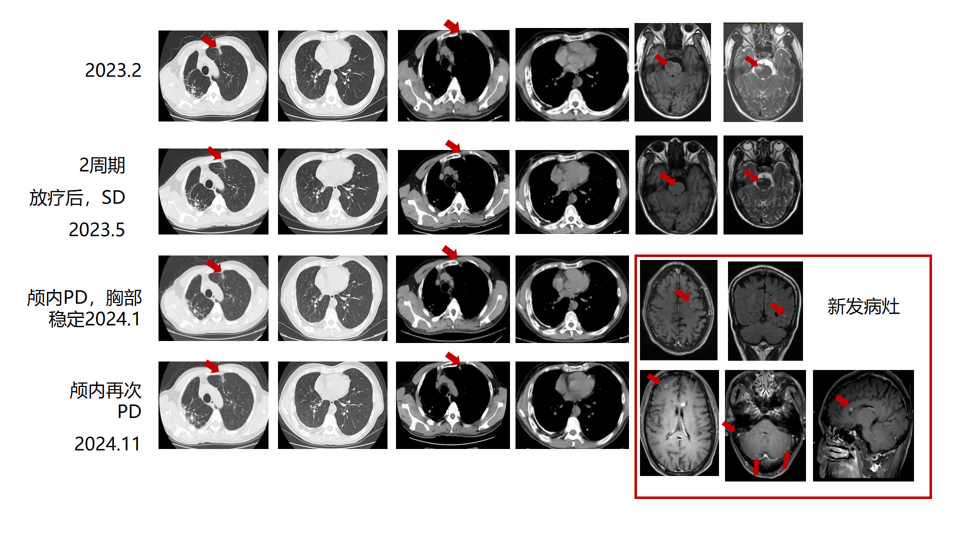
图7. 二线治疗前后影像学评估结果
■三线治疗
治疗方案:2024年11月至2025年7月,行德曲妥珠单抗+信迪利单抗治疗9周期。
疗效评估:2周期、4周期、7周期后均评估为PR(2周期后脑内肿瘤完全消失,胸部病灶稳定),PFS超过8个月。
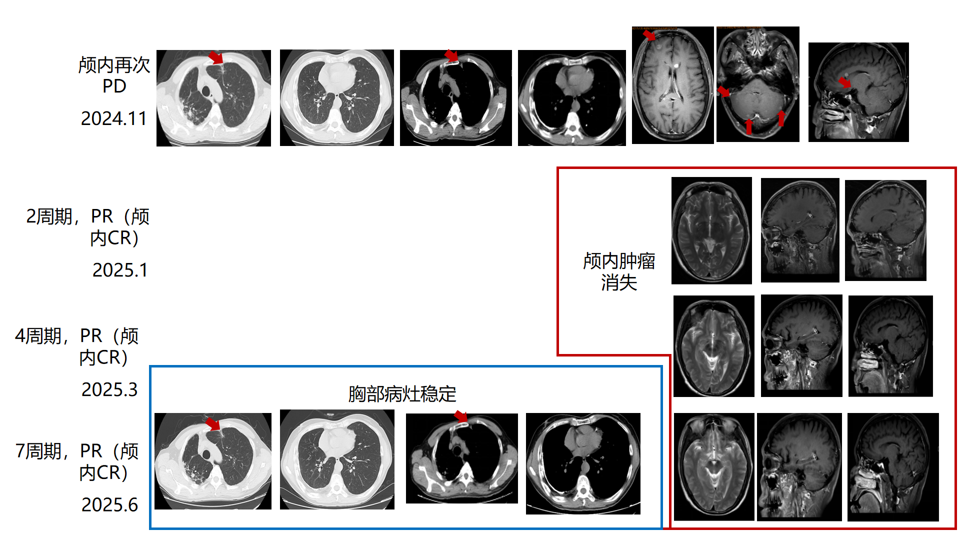
图8. 三线治疗前后影像学评估结果
■病例总结
患者男性,左肺低分化腺癌,IV期(双肺、胸膜、淋巴结、脑转移)。基因检测提示EGFR L858R突变伴ERBB2扩增/STARD3-ERBB2融合。
一线使用白蛋白紫杉醇+顺铂+吉非替尼联合治疗4周期后吉非替尼维持,2周期评估达PR,PFS达21个月;后因脑转移进展评估为PD。
二线使用奥希替尼80mg(后增量至160mg)联合脑部放疗,维持SD状态20个月,最终因颅内多发进展评估为PD。
三线接受德曲妥珠单抗+信迪利单抗联合治疗,2周期即达PR(颅内病灶消失),目前已维持PR状态超过8个月,总生存期(OS)超过50个月。治疗全程耐受性良好,未出现严重不良反应。
专家点评
HER2变异作为NSCLC的重要治疗靶点,其变异形式多样(包括突变、扩增及融合),针对HER2变异的精准治疗策略始终是临床关注的焦点。近年来,ADC药物德曲妥珠单抗通过DESTINY-Lung系列研究,在HER2变异晚期NSCLC中展现出突破性疗效。本文报道的两例复杂病例,从真实世界角度印证了德曲妥珠单抗的卓越疗效,并深化了对其作用机制的理解。
病例1为67岁男性左肺腺癌伴多发转移,基因检测为ERBB2 pD277Y(35.32%),免疫组化为HER2 2+。一线奥希替尼治疗,二线奥希替尼+吡咯替尼治疗进展后,采用奥希替尼+德曲妥珠单抗治疗10周期,2周期即达PR,并维持PR,治疗过程中总体耐受性良好,三线PFS达11个月,随后又经第三代EGFR-TKI联合化疗等多线治疗进展后,采取贝伐珠单抗+甲氨蝶呤O囊注入+奥希替尼+赛沃替尼治疗,目前患者自述状态较前好转,持续获益中。这一成功实践与DESTINY-Lung01(DL01)研究高度吻合,该研究显示德曲妥珠单抗在HER2突变(含融合亚型)NSCLC中的客观缓解率(ORR)达55%[3]。此外,2024年AACR首次披露的DESTINY-Lung05(DL05)研究数据提示,德曲妥珠单抗在中国HER2突变晚期NSCLC患者中单药ORR高达58.3%[4],而本例通过联合第三代EGFR-TKI实现疗效再提升,为HER2变异晚期NSCLC患者提供了治疗思路。
病例2(多驱动共突变伴脑转移)为晚期肺腺癌男性患者,存在EGFR L858R突变+HER2扩增/STARD3-HER2融合,伴脑转移。前两线治疗(化疗+EGFR-TKI、奥希替尼增量+放疗)累计PFS达41个月,最终因颅内进展耐药。三线采用德曲妥珠单抗联合信迪利单抗后,2周期颅内病灶消失,全身疗效评估达PR,持续缓解>8个月,OS突破50个月,且耐受性优异,目前仍在持续获益中。这一卓越疗效获得三重循证支持:首先,Ⅱ期HERALD/EPOC1806研究展现出德曲妥珠单抗在HER2扩增实体瘤中的治疗潜力,研究者评估的ORR为56.5%,中位缓解持续时间(DoR)为8.8个月[5],而本例通过德曲妥珠单抗+PD-1抑制剂或可绕过EGFR通路耐药,为这类患者带来治疗获益;其次,DESTINY-Lung01/02脑转移汇总分析证实,德曲妥珠单抗的颅内客观缓解率(IC-ORR)高达50%,颅内中位缓解持续时间(IC-DoR)达9.5个月[6],本例2周期颅内CR与此高度一致;最后,DL05中国桥接中德曲妥珠单抗组12个月PFS率达55.1%[4],本例OS>49个月印证了其对复杂变异患者的生存重塑能力。
这两个病例不仅验证了DESTINY-Lung系列核心数据,更拓展了德曲妥珠单抗在罕见融合、多线耐药及脑转移中的应用边界。
精准检测是优化治疗的基础,本文两例患者均通过基因检测成功识别基因融合及共突变,印证了2025版CSCO指南将HER2突变检测上调至I级推荐,并首次将HER2过表达检测纳入推荐体系(III级推荐)的必要性[7]。在联合策略方面,病例1中德曲妥珠单抗联合第三代EGFR-TKI为多线经治患者带来疗效提升,病例2中德曲妥珠单抗与PD-1抑制剂的协同作用克服多线耐药,为复杂变异患者提供了新治疗范式;目前DESTINY-Lung06研究(NCT05638209)正在探索德曲妥珠单抗±免疫化疗一线治疗的潜力。此外,关键III期DESTINY-Lung04研究(NCT05048797)直接比较德曲妥珠单抗与化疗在HER2突变NSCLC一线治疗的疗效,期待随着更多研究结果的公布,为HER2变异NSCLC的全程管理格局带来更优的策略方法。
专家简介

王李杰 教授
肿瘤学博士
解放军总医院肿瘤内科副主任医师
中国老年保健协会胸部肿瘤精准治疗分会副主任委员
北京慢性病防治与健康教育研究会肺癌专委会副主任委员
中国研究型医院学会分子肿瘤免疫专业委员会委员
中国研究型医院学会肿瘤专业委员会委员
北京肿瘤学会肺癌专业委员会常务委员
北京癌症防治学会肺癌免疫治疗专业委员会常务委员
北京肿瘤防治研究会免疫分委会委员
北京医学奖励基金会肺癌医学青年委员会委员
承担参与国家、全军及省部级科研项目多项,发表论文40余篇,参编专著8部
专家简介

刘庆艳 教授
博士,解放军总医院肿瘤医学部肿瘤内科,主治医师
以第一作者在
BMC Medicine等TOP期刊发表多篇SCI论文,参与多项国家及省部级课题
参考文献:
[1] Han B, et al. Cancer incidence and mortality in China, 2022. J Natl Cancer Cent. 2024;4(1):47-53.
[2] Cooper AJ, et al. Human Epidermal Growth Factor Receptor 2-Mutant Non-Small-Cell Lung Cancer: Continued Progress But Challenges Remain. J Clin Oncol. 2022 Mar 1;40(7):693-697.
[3] Li BT, et al. Trastuzumab Deruxtecan in HER2-Mutant NSCLC: DESTINY-Lung01. NEJM. 2022;387:545-554.
[4] Cheng Y, et al. Trastuzumab deruxtecan (T-DXd) in Chinese patients (pts) with previously treated HER2 mutant non-small cell lung cancer (NSCLC): primary analysis from the Phase 2 DESTINY-Lung05 (DL-05) trial. 2024 AACR. CT248.
[5] Yagisawa M, et al. Trastuzumab Deruxtecan in Advanced Solid Tumors With Human Epidermal Growth Factor Receptor 2 Amplification Identified by Plasma Cell-Free DNA Testing: A Multicenter, Single-Arm, Phase II Basket Trial. J Clin Oncol. 2024 Aug 1:JCO2302626.
[6] Li BT, et al. T-DXd in HER2-Mutant NSCLC with Brain Metastases: Pooled Analysis of DL01/02. 2023 ESMO 1321MO.
[7] 中国临床肿瘤学会(CSCO)非小细胞肺癌诊疗指南(2025年).
* 此文仅用于向医学人士提供科学信息,不代表本平台观点
亿赢配资网提示:文章来自网络,不代表本站观点。



